Investigadores del Instituto de Neurociencias, centro mixto de la Universidad Miguel Hernández (UMH) y el Consejo Superior de Investigaciones Científicas (CSIC), han obtenido por primera vez imágenes de la activación de la microglía y de los astrocitos, dos tipos de células involucradas en la neuroinflamación, mediante resonancia magnética ponderada por difusión.

Este importante avance, desarrollado en ratas y probado en humanos sanos, podría transformar la investigación básica y clínica, y permitir estudiar de manera no invasiva y longitudinal el papel de la inflamación cerebral en Alzheimer, Parkinson o esclerosis múltiple y proporcionar valiosos biomarcadores tempranos de estas enfermedades neurodegenerativas.
En la actualidad no existen técnicas de imagen no invasivas capaces de caracterizar específicamente la inflamación cerebral in vivo. La técnica de elección actual, la tomografía por emisión de positrones (PET), requiere exposición a la radiación y es difícil de generalizar.
Una investigación conjunta de los laboratorios dirigidos por Silvia de Santis y Santiago Canals, ambos del Instituto de Neurociencias UMH-CSIC, ha permitido visualizar por primera vez y con gran detalle la inflamación cerebral, utilizando Resonancia Magnética Ponderada por difusión. Esta detallada ‘radiografía’ de la inflamación no puede obtenerse con una resonancia magnética convencional, sino que requiere secuencias de adquisición de datos y modelos matemáticos especiales.
Las claves de esta innovadora técnica
Una estrategia innovadora desarrollada en el campus de Sant Joan de la UMH ha hecho posible este importante avance, que publica la revista Science Advances y que puede ser crucial para cambiar el rumbo del estudio y tratamiento de las enfermedades neurodegenerativas.
La investigación, cuya primera autora es Raquel García Hernández, demuestra que la Resonancia Magnética ponderada por difusión puede detectar de forma no invasiva y diferenciada la activación de la microglía y los astrocitos, dos tipos de células del cerebro que están en la base de la neuroinflamación y su progresión.
Las enfermedades cerebrales degenerativas como Alzheimer y otras demencias, Parkinson o esclerosis múltiple son un problema acuciante y difícil de abordar. La activación sostenida de dos tipos de células del cerebro, la microglía y los astrocitos conduce a una inflamación crónica en el cerebro que es una de las causas de la neurodegeneración y contribuye a su progresión.
Las desventajas de este método
Sin embargo, hay una carencia de enfoques no invasivos capaces de caracterizar específicamente la inflamación en cerebros de sujetos vivos. El estándar de oro actual es la tomografía por emisión de positrones (PET), pero es difícil de generalizar y está asociada a exposición a la radiación ionizante, por lo que su uso está limitado en poblaciones vulnerables y en estudios longitudinales, que requieren el uso de PET de manera repetida durante un período de años, como es el caso de las enfermedades neurodegenerativas.
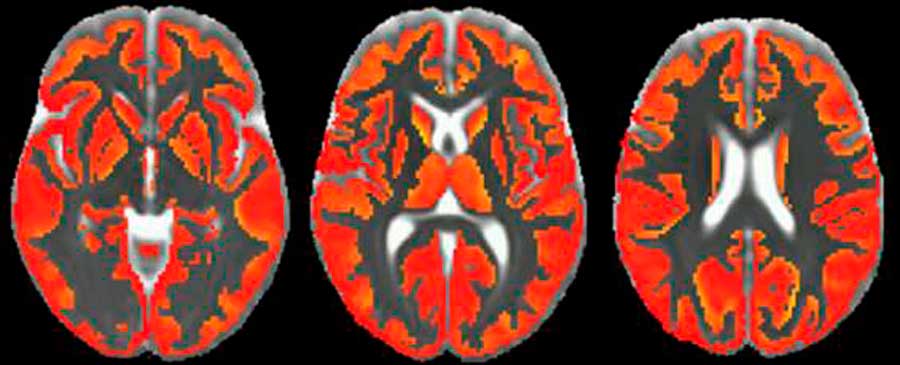
Otro inconveniente del PET es su baja resolución espacial, que la hace inadecuada para obtener imágenes de estructuras pequeñas, con el inconveniente añadido de que los radiotrazadores específicos de la inflamación no distinguen el tipo de célula (microglía, astrocitos y endotelio).
Frente a estos inconvenientes, la resonancia magnética ponderada por difusión tiene la capacidad única de obtener imágenes de la microestructura cerebral in vivo de forma no invasiva y con alta resolución, al capturar el movimiento aleatorio de las moléculas de agua en el parénquima cerebral para generar contraste en las imágenes de resonancia magnética.
Este trabajo ha logrado demostrar, también, el valor traslacional del enfoque utilizado en una cohorte de humanos sanos a alta resolución, “en la que realizamos un análisis de reproducibilidad. La asociación significativa con patrones de densidad de microglía conocidos en el cerebro humano apoya la utilidad del método para generar biomarcadores de glía fiables.
Creemos que caracterizar así aspectos relevantes de la microestructura tisular durante la inflamación, de forma no invasiva y longitudinal, puede tener un tremendo impacto en nuestra comprensión de la fisiopatología de muchas afecciones cerebrales, y puede transformar la práctica diagnóstica actual y las estrategias de seguimiento del tratamiento de las enfermedades neurodegenerativas”, destaca la investigadora Silvia de Santis.