Investigadores de la Universidad de Granada (UGR), en colaboración con la Universidad de Sevilla, han ensayado con éxito en cultivos de células tumorales de cáncer de pulmón y en modelos de ratones una nueva fórmula para administrar el fármaco paclitaxel transportándolo en nanopartículas desarrolladas a partir de un copolímero de ácido láctico y ácido glicólico
Los resultados de este trabajo han sido publicados en la prestigiosa revista Pharmacological Research.
El paclitaxel (Taxol) es un agente muy efectivo para el tratamiento del cáncer de pulmón y mama, pero presenta una importante limitación en su uso: induce intenso dolor al lesionar las neuronas sensitivas que se localizan en los ganglios espinales (neuropatía periférica), lo que provoca en muchas ocasiones la suspensión del tratamiento.
Además, paclitaxel es un fármaco no selectivo con alta toxicidad, que necesita para su administración excipientes que pueden provocar efectos secundarios graves. Por último, su efectividad es menor en las denominadas cáncer stem cells, células tumorales resistentes a este y otros fármacos y que son responsables de la reaparición de la enfermedad.
La labor de investigación liderada por José Carlos Prados, catedrático del departamento de Anatomía y Embriología Humana y miembro de Centro de Investigación Biomédica (CIBM) de la UGR y del Instituto de Investigación Biosanitaria ibs.Granada, y Lucía Martín Banderas, profesora titular del departamento de Farmacia y Tecnología Farmacéutica de la Universidad de Sevilla, ha sido desarrollada dentro de un Proyecto de Investigación de Excelencia dirigido por el profesor José Manuel Baeyens, catedrático del departamento de Farmacología y también miembro del CIBM de la UGR y del ibs.Granada.
El proyecto ha contado con la colaboración de investigadores del Instituto de Investigación Biosanitaria y el Hospital Universitario Virgen de las Nieves de Granada.
Efecto protector
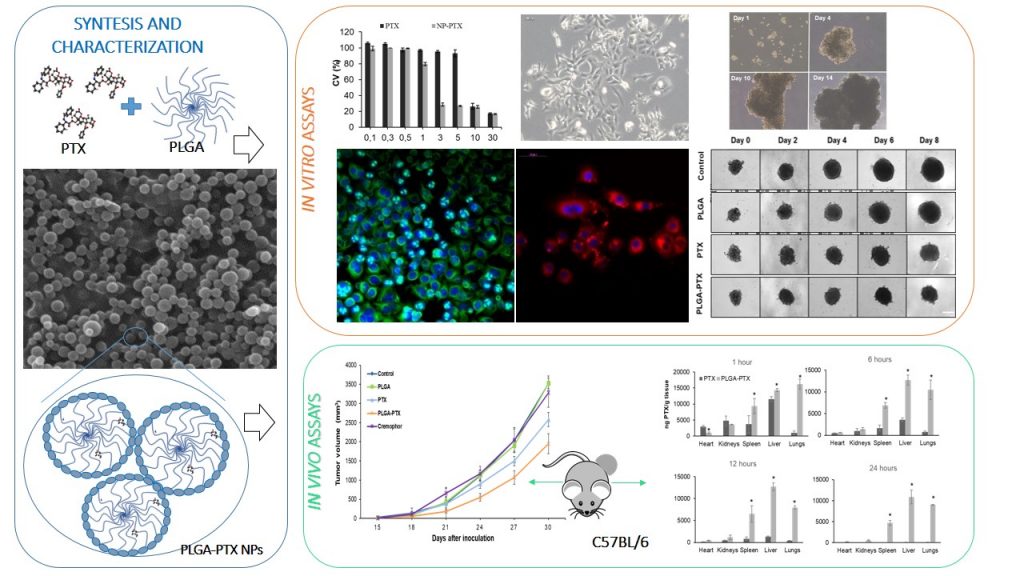
Los estudios llevados a cabo han demostrado por primera vez que la asociación del agente paclitaxel a una nueva nanopartícula de ácido láctico y ácido glicólico no sólo presenta una alta biocompatibilidad, lo que es esencial para su uso en humanos, y es capaz de aumenta la actividad del fármaco sobre las células madre tumorales, sino que podría ejercer un efecto protector contra la neuropatía periférica.
Los resultados ‘in vivo’ utilizando ratones han demostrado un aumento en el tiempo de circulación del fármaco y una mayor acumulación en los tejidos pulmonares y cerebrales, lo que podría representar una ventaja para su utilización.
Pero además, los niveles de fármaco detectados en los ganglios de la raíz dorsal espinal son extremadamente bajos, lo que evitaría el desarrollo de dolor neuropático. Los últimos estudios de los grupos de investigación implicados intentan determinar el mecanismo por el que el nuevo nanofármaco protege del desarrollo de la neuropatía periférica, lo que será objeto de una nueva publicación en breve.