Investigadores colombianos desarrollan una tecnología médica que usa nanofluidos magnéticos —líquidos con diminutas partículas— para aplicar calor directo sobre los tumores y hacer más efectivos los tratamientos contra el cáncer.
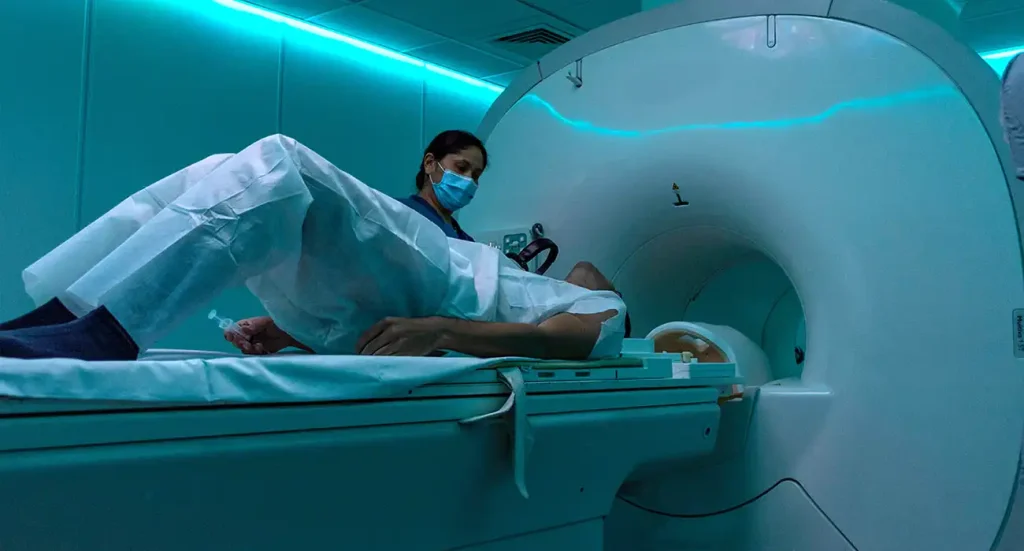
Esta técnica, llamada hipertermia magnética, consiste en elevar la temperatura de los tejidos tumorales a entre 43 y 46 °C mediante campos magnéticos aplicados a nanopartículas.
Su éxito conseguiría reducir hasta en un 50 % los ciclos de quimio o radioterapia.
El proyecto es liderado por el grupo de investigación en Mecánica Aplicada de la Facultad de Minas de la Universidad Nacional de Colombia (UNAL) Sede Medellín, con la dirección del profesor Néstor Ricardo Rojas Reyes. Este equipo ha consolidado una alianza estratégica para fortalecer la investigación institucional en el desarrollo de nanofluidos magnéticos aplicables en hipertermia como alternativa terapéutica en tratamientos oncológicos.
Los nanofluidos magnéticos son líquidos que contienen partículas microscópicas de materiales con comportamiento super-paramagnético –como la magnetita o la maghemita– que dispersos forman una mezcla homogénea. Por su diminuto tamaño y su capacidad de responder a campos magnéticos alternos, estas partículas generan calor localizado dentro del cuerpo humano.
Dicha propiedad es esencial en la hipertermia magnética, ya que posibilita calentar exclusivamente el tejido tumoral sin afectar las células sanas circundantes. Para lograrlo, los investigadores deben garantizar que los nanofluidos sean estables, es decir que las partículas no se agreguen ni cambien sus propiedades con el tiempo.
La iniciativa busca no solo avanzar en la aplicación clínica de esta técnica sino también fomentar la autonomía tecnológica del país en el ámbito de la salud. “Al desarrollar capacidades locales en la producción y aplicación de nanofluidos magnéticos se pretende reducir la dependencia de tecnologías importadas y mejorar el acceso a tratamientos innovadores para la población colombiana”, señala el profesor Rojas.
El contexto global también da cuenta de la urgencia de estos avances, pues según la Organización Mundial de la Salud (OMS) cada año más de 20 millones de personas en el mundo son diagnosticadas con algún tipo de cáncer, y al menos 10 millones mueren por esta causa. En Colombia la enfermedad representa una de las principales causas de muerte, y el acceso a tratamientos sigue condicionado por altos costos, centralización del servicio y dependencia tecnológica.
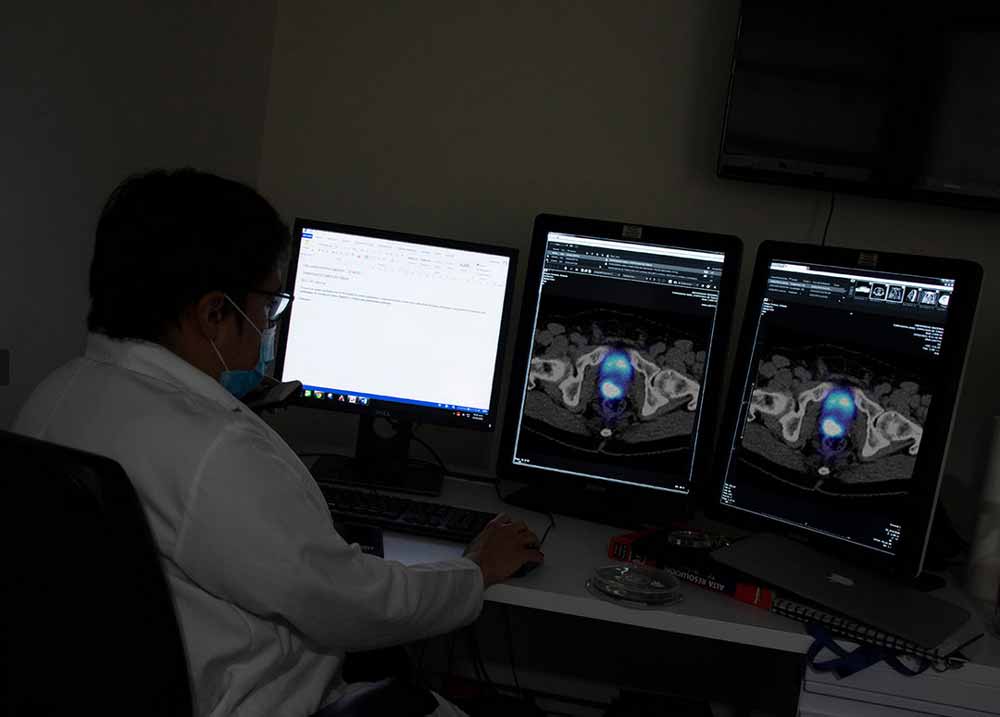
En ese sentido, “tratamientos como la hipertermia magnética representan una opción innovadora que complementaría las terapias existentes y ampliaría el acceso a soluciones más personalizadas y efectivas”, afirma la investigadora Laura Carolina Álvarez Gil, de la Facultad de Minas, estudiante del Doctorado en Ingeniería – Ciencia y Tecnología de Materiales.
Esta técnica consiste en elevar la temperatura de los tejidos tumorales a entre 43 y 46 °C mediante campos magnéticos aplicados a nanopartículas. A esa temperatura las células cancerosas se vuelven más vulnerables a tratamientos como la quimio o la radioterapia, permitiendo reducir su intensidad sin comprometer su eficacia. Su ventaja sobre otros métodos es la precisión: al concentrarse solo en la zona afectada minimiza el daño a los tejidos sanos circundantes.
“Es comparable con la respuesta natural del cuerpo ante infecciones: el aumento de la temperatura afecta la supervivencia de ciertos organismos o células”, explica la investigadora.
Infraestructura robusta construida desde cero

El proyecto se ha consolidado en varias líneas de acción complementarias. Una de ellas es el desarrollo de modelos computacionales que permiten predecir la temperatura alcanzada por los nanofluidos al someterlos a campos magnéticos, incorporando variables como el tamaño de la partícula, el tipo de recubrimiento y las condiciones del campo aplicado.
“Hasta ahora hemos encontrado una alta dependencia entre la concentración de nanopartículas y la respuesta térmica, pero debemos seguir incorporando otras variables para robustecer los modelos que usamos y estimar cuánta energía se entrega al sistema”, añade.
Paralelamente el equipo ha formulado nanofluidos estables utilizando nanopartículas de magnetita fabricadas localmente. Para mejorar su calidad y funcionamiento se han aplicado métodos que permiten evitar que las partículas se agreguen, lo cual afectaría su desempeño. Estos incluyen el uso de vibraciones ultrasónicas (sonicación) y ajustes en el nivel de acidez del líquido (pH) que ayudan a mantener la mezcla homogénea y a optimizar su capacidad de generar calor.
“Al inicio del proyecto no contábamos con infraestructura ni materiales especializados. Logramos construir desde cero una infraestructura robusta y adecuada para formular, caracterizar y evaluar el desempeño térmico de los nanofluidos”, resalta la investigadora Álvarez.
Otro componente fundamental ha sido el diseño de modelos tipo phantom, bloques de gel que simulan tejidos humanos y permiten estudiar la distribución del calor generado por los nanofluidos, incluso en condiciones que replican la circulación de fluidos y la presencia de interfaces complejas.
“Estos modelos físicos nos permiten visualizar la distribución del calor en condiciones más cercanas a las reales, incluyendo interfaces entre tejidos o la circulación de fluidos”, añade.
Por último, mediante termografía infrarroja, una herramienta no invasiva, el equipo ha podido visualizar en tiempo real cómo se propaga el calor en estos modelos, lo que ha sido fundamental para validar sus simulaciones computacionales y ajustar las condiciones experimentales.
Aunque el desarrollo apenas lleva año y medio ya cuenta con una infraestructura sólida y avances metodológicos importantes. La siguiente fase será validar la biocompatibilidad de los nanofluidos in vitro, o en laboratorio, en alianza con otros grupos de investigación de la región, para considerar posteriormente ensayos en modelos animales.
En Colombia hoy no existen dispositivos funcionales para la aplicación clínica de esta técnica, a pesar de que en Europa y Estados Unidos ya se explora con éxito.
“Producir localmente esta tecnología permitiría agilizar el acceso a tratamientos más económicos y personalizados, no solo para cáncer sino para otras enfermedades tratables con calor localizado”, concluye.
Este esfuerzo ha sido posible gracias a una alianza interdisciplinaria que articula el trabajo de los grupos de investigación en Promoción e Investigación en Mecánica Aplicada (GPIMA), en Materiales Cerámicos y Vítreos, en Biotecnología Animal (GIBA), Computational Applications (PCM), en Nanoestructuras y Física Aplicada (Nanoupar), además de la empresa Cecoltec Services y el Instituto de Minerales (Cimex).
















