Un equipo de la Universidad de Castilla-La Mancha (UCLM) ha desarrollado un modelo matemático para estudiar el comportamiento celular y descubren que un tipo de células adoptan una conducta concreta asociada a enfermedades cardiovasculares.

Investigadores del Laboratorio de Oncología Matemática (MOLAB) de la Universidad de Castilla-La Mancha (UCLM), a partir del desarrollo de un modelo matemático basado en técnicas de redes complejas e inteligencia artificial, y en colaboración con investigadores del Centro Nacional de Investigaciones Cardiovasculares Carlos III (CNIC), liderados por Andrés Hidalgo, han descubierto que los neutrófilos, un tipo de células inmunes, adquieren diferentes ‘comportamientos’ en la sangre durante procesos inflamatorios. El estudio, publicado en la prestigiosa revista Nature, ha logrado identificar una conducta asociada con enfermedades cardiovasculares.
El trabajo, que ha combinado la modelización matemática y el análisis masivo de datos morfológicos y dinámicos provenientes de imágenes 4D in vivo de más de cien mil células inmunes obtenidas por el CNIC, tiene una gran relevancia desde el punto de vista terapéutico, ya que puede permitir el diseño de nuevos tratamientos para minimizar las secuelas ocasionadas por los infartos de miocardio, tal y como explica Gabriel Fernández Calvo, profesor del Departamento de Matemáticas de la UCLM, investigador de MOLAB y coautor del estudio.
Relación entre los neutrófilos y las enfermedades cardiovasculares
Los neutrófilos son un tipo de células inmunes que constituyen la principal línea de defensa del organismo, pero también pueden ocasionar daños a células sanas, sobre todo del sistema cardiovascular. Numerosos estudios previos han asociado que una elevada presencia de neutrófilos en sangre aumenta el riesgo y severidad de padecer problemas cardiovasculares. Sin embargo, no es posible la eliminación de neutrófilos para proteger el sistema cardiovascular, ya que se generaría un estado de indefensión ante distintos patógenos, lo cual sería contraproducente para el organismo.
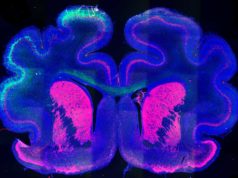
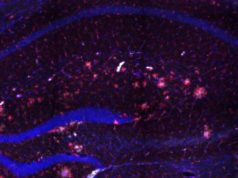
Para resolver esta paradoja, los autores buscaron identificar tipos específicos de neutrófilos responsables del daño vascular. Para ello, analizaron el comportamiento de las células utilizando microscopía intravital de alta resolución (tecnología que permite visualizar células dentro de los capilares sanguíneos en animales vivos). Por ello, diseñaron un sistema computacional altamente novedoso capaz de analizar cómo se comportan las células inmunes en los vasos sanguíneos mediante mediciones simples en los cambios de tamaño, forma y movimiento que experimentan tales células.
Así, descubrieron que las células inmunes presentan tres patrones de comportamiento durante el transcurso de los procesos inflamatorios, pero solo uno estos patrones de comportamiento, caracterizado por un mayor tamaño y proximidad a las paredes de los vasos, estaba asociado a daño cardiovascular.
Mediante análisis genéticos masivos en modelos animales, utilizaron este sistema computacional para encontrar moléculas responsables de esos comportamientos patológicos en neutrófilos que conducían al daño cardiovascular. Uno de los principales hallazgos del estudio fue la identificación de una molécula, denominada Fgr, que es responsable de ese comportamiento patológico de los neutrófilos, lo que a su vez fue clave para seleccionar un fármaco de gran eficacia para prevenir la inflamación y la muerte celular tras un infarto de miocardio.
“Uno de los aspectos más novedosos del estudio es que, mediante la combinación de una tecnología de extracción de imágenes 4D in vivo procedentes de miles de células y de técnicas matemáticas de análisis masivo de datos, se abre la puerta para que, en un futuro, se pueda utilizar esta estrategia metodológica para identificar nuevas dianas moleculares y con ello diseñar tratamientos más específicos en pacientes”, tal y como indica David G. Aragonés González, estudiante de doctorado del Departamento de Matemáticas de la UCLM e investigador de MOLAB.
“La idea ahora es aplicarlo a otros escenarios no solo infecciosos sino, también, en tumores. En estos últimos existe una fuerte interacción entre las células del sistema inmune y las células tumorales. Debido a la enorme heterogeneidad que muestran muchos cánceres, será muy interesante poder caracterizar dinámicamente los procesos clave que entran en juego y hacerlo con una resolución espacio-temporal sin precedentes”, señala Gabriel Fernández Calvo.
En este estudio multidisciplinar han colaborado Behavioral immune landscapes of inflammation, el Centro Nacional de Investigaciones Cardiovasculares Carlos III, la Agencia de Ciencia y Tecnología de Singapur (ASTAR), Vithas Hospitales en Madrid, las Universidades de Yale, Harvard, Baylor y Carlos III. Por parte de la UCLM, han sido coautores los investigadores de MOLAB David G. Aragonés González, estudiante de doctorado, y Gabriel Fernández Calvo, profesor del Departamento de Matemáticas.
El trabajo ha sido publicado el 5 de enero de 2022 en la revista Nature https://www.nature.com/articles/s41586-021-04263-y, perteneciente a la categoría de Ciencias Multidisciplinares, con un índice de impacto de 49.962 y posición Q1 (1/72).