Los efectos letales del monóxido de carbono son de sobra conocidos. Este gas, generado principalmente por una mala combustión, es el responsable de la llamada ‘muerte dulce’, porque sume a sus víctimas en un sueño del que no pueden escapar. Es un gas incoloro, inodoro e imposible de detectar si no se cuentan con los medios técnicos adecuados. Sin embargo, este gas letal si se respira también tiene un lado positivo y se puede emplear en el desarrollo de nuevos fármacos para la lucha contra el cáncer, como estudia un equipo de la Universidad de Jaén (UJA).

Las investigadoras del Departamento de Química Inorgánica y Orgánica de la UJA, Sonia Jiménez y Nuria Illán, trabajan en el desarrollo y síntesis de compuestos metálicos en los que se incluyen moléculas de monóxido de carbono, con el objetivo de comprobar su efectividad en el tratamiento del glioblastoma, el tumor del cerebro más letal y para el que todavía no se cuenta con una estrategia de abordaje efectiva.
Por qué el monóxido de carbono puede servir para tratar el cáncer
Desde hace más de treinta años se conoce que, aparte de ser un gas letal, el monóxido de carbono interviene en algunos procesos biológicos relacionados con una gran variedad de enfermedades, así como que la aplicación de este gas ayuda a revertirlos y frenar los desajustes orgánicos propios de algunas patologías. Sin embargo, no se había resuelto cómo dispensarlo en el organismo, porque si se realizaba de una manera poco controlada y en una dosis excesiva, el efecto negativo que podría provocar en el organismo sería mucho más grave que la enfermedad que se desea paliar. Y solamente se podía emplear a unas dosis muy bajas, con lo que se perdía buena parte de su potencial terapéutico.
Años después se descubrió que como el monóxido de carbono se unía a metales, se podrían diseñar compuestos capaces de transportarlo y liberarlo de manera controlada, así como convertirlo en un elemento sólido. Este método hace posible aplicar dosis mayores y aprovechar toda su capaciad terapéutica, al tiempo que se elminina la posibilidad de dañar partes sanas del organismo.
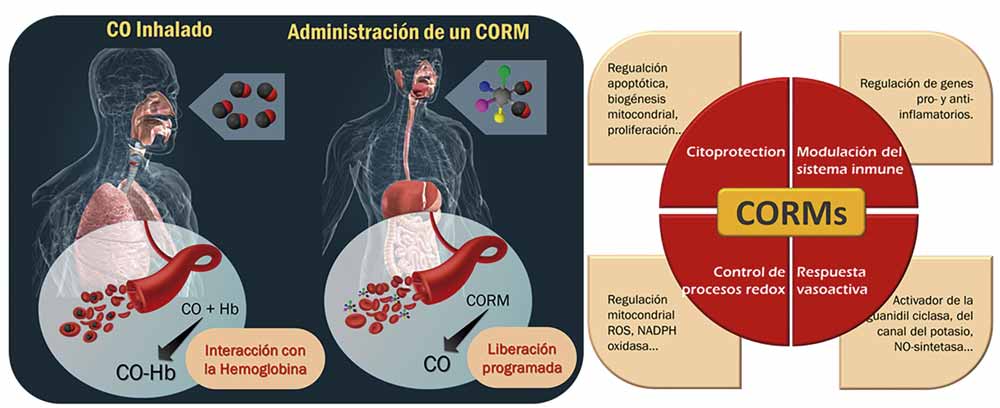
Qué avance en la aplicación del monóxido de carbono contra el cáncer se ha desarrollado en la UJA
A partir de estos resultados, Nuria Illán y Sonia Jiménez se plantearon probar este tipo de compuestos para combatir el cáncer e iniciaron un trabajo de síntesis y caracterización de una serie de compuestos metálicos con monóxido de carbono, que les ha llevado a desarrollar hasta 25 formulaciones distintas en las que está presente este gas en estado sólido. Las investigadoras de la UJA admiten que no todas ellas funcionan de la manera que se esperaban, pero consideran que son un punto de partida interesante para seguir esta línea de investigación y desarrollar síntesis más efectivas.
Para alcanzar el éxito y atacar a la célula, los compuestos metálicos deben ser lo suficientemente estables para mantenerse inalterados en su viaje por el organismo, hasta alcanzar el objetivo fijado, que en este caso era el cerebro. Y una vez ante el objetivo, deben provocar la reacción química que permite la liberación del monóxido de carbono.
Como es de imaginar, controlar todas estas reacciones no resulta nada sencillo, pero Nuria Illán y Sonia Jiménez han logrado acercarse bastante al objetivo fijado al inicio del proyecto de investigación, que ha contado con financiación procedente de fondos FEDER, así como colaboraciones con grupos de otras universidades, a través de la Red METALBIO.
Cómo ataca este gas a los tumores: todavía es una incógnita
De partida, este proyecto plantea una incógnita que todavía no se ha podido resolver. Se sabe que el monóxido de carbono funciona contra el cáncer, pero no se conoce exactamente si su acción se debe a su capacidad para intervenir en los procesos celulares e interferir en la reproducción de las células o si daña a las células del tumor por su toxicidad. Sin embargo sí que está claro, explican las investigadoras de la UJA, que el daño producido en las células tumorales se debe exclusivamente al monóxido de carbono y no al metal al que está unido, porque las moléculas metálicas tienen un tamaño que no le permiten atravesar la barrera celular.
Para que las moléculas de monóxido de carbono puedan acceder al interior de las células se necesita una llave especial o, mejor dicho, establecer una especie de intercambio de compuestos con la célula, mediante una reacción química. «Tratamos de que los compuestos que sintetizamos reaccionen con el medio donde se encuentran, para que se libere ese monóxido de carbono -de la síntesis creada por las investigadoras- y pueda introducirse en la célula», explica Sonia Jiménez.
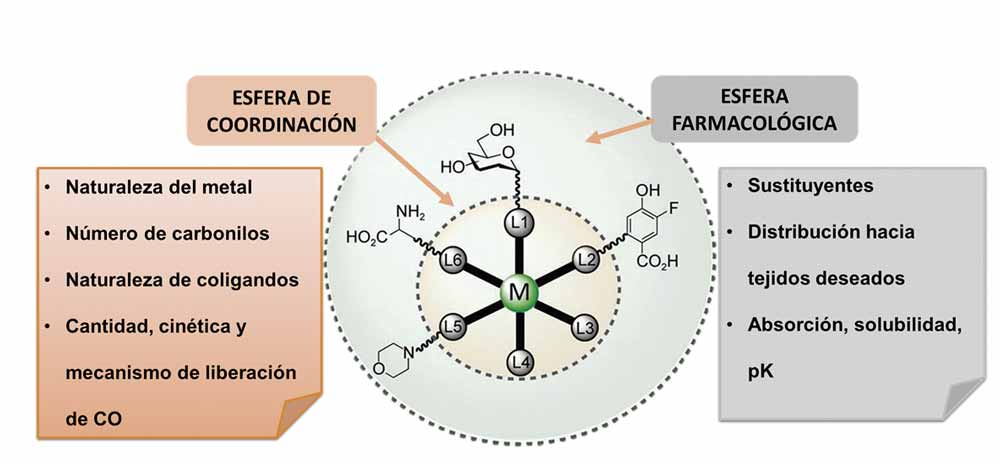
Sin embargo, no basta con que las moléculas de monóxido de carbono accedan a la célula sin más, sino que deben hacerlo de manera controlada, para que se produzca el efecto terapéutico deseado. Los complejos metálicos diseñados por Nuria Illán y Sonia Jiménez están hechos con renio, al que se le añaden un seis elementos más. «Modulando esos compuestos podemos hacer que sean solubles o no, que los enlaces entre el metal y el monóxido de carbono sean más fuertes o más débiles para que la liberación sea más rápida o más lenta», aclara Sonia Jiménez.
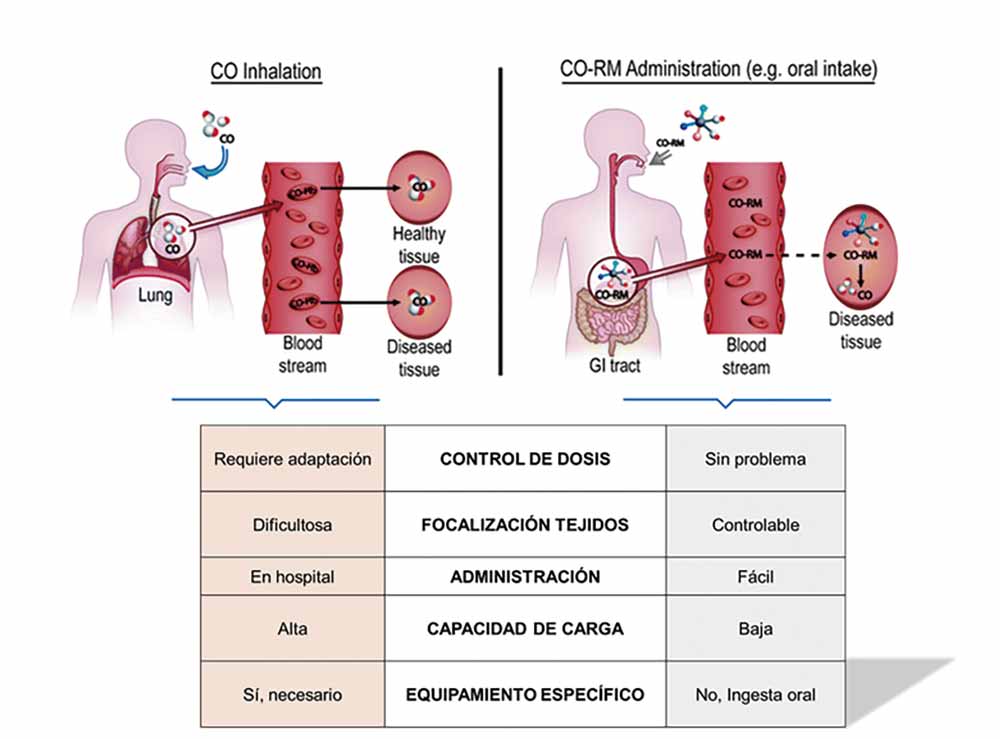
Cuál es el principal escollo en el uso del monóxido de carbono contra el cáncer
La parte de la liberación controlada de las moléculas de monóxido de carbono ha sido el principal escollo en este proyecto, porque las posibilidades de combinación son tan elevadas, que dar con la fórmula adecuada se complica. Incluso, en algunas de las pruebas, dicen las investigadoras de la UJA, cuando teóricamente y con los cálculos realizados previamente todo apuntaba a que iba a funcionar, en las pruebas realizadas in vitro se ha comprobado que la liberación del monóxido de carbono no se realizaba al ritmo previsto en un principio, y no se alcanzaban los objetivos del experimento. De ahí que todavía continúa pendiente dar con unas moléculas que al formar estos compuestos con renio y monóxido de carbono liberen el gas de manera adecuada.
Nuria Illán aclara que en los experimentos han empleado análogos de biomoléculas, «concretamente trabajamos con derivados de uracilo, que es una de las bases primidínicas que se encuentra en el ARN y también trabajamos con pteridinas», con el objetivo de que el organismo no las trate como elementos extraños y les permita ejercer su trabajo.
Qué condiciones deben tener estas síntesis para tratar los tumores
Otra cuestión clave ha estado relacionada con las condiciones de compuestos, que deben contar con «una buena estabilidad termodinámica y cinética», dice Nuria Illán, para que lleguen a su destino en las condiciones adecuadas, sin que hayan sufrido cambios en su estructura química.
En el proyecto han participado grupos de tres departamentos de la UJA, que han trabajo de forma coordinada. Por un lado, desde el Departamento de Química Inorgánica y Orgánica, Sonia Jiménez y Nuria Illán se han encargado del estudio de la caracterización de los compuestos, para conocer cómo se pueden comportar; el Departamento de Química Física y Analítica se ha centrado en realizar los cálculos teóricos, para ver cómo se modula o cómo se libera el monóxido de carbono, a fin de aclarar el factor del que depende la liberación del gas y se pueda regular a medida, para hacerla más efectiva; por último, investigadores del Departamento de Biología, han aplicado las moléculas a células de tumor cerebral, para conocer cómo se comportan y sacar conclusiones para nuevas síntesis.
Este proyecto de investigación no ha cosechado los resultados esperados, pero sí ha demostrado que esta línea de trabajo resulta muy interesante para tratar los glioblastomas, unos tumores que se comportan diferente al restos y cuyo tratamiento todavía es una asignatura pendiente para la ciencia.















