Un equipo de investigación del Centro Andaluz de Biología del Desarrollo (CABD) ha identificado un mecanismo innovador que podría abrir nuevas vías terapéuticas para la enfermedad neurodegenerativa BPAN (Beta-Propeller Protein-Associated Neurodegeneration).

El estudio, liderado por el catedrático de Biología Celular de la Universidad Pablo de Olavide José Antonio Sánchez Alcázar y publicado en International Journal of Molecular Sciences, demuestra que la biotina, un nutriente con propiedades epigenéticas, puede reactivar el cromosoma X inactivo y restaurar funciones celulares alteradas en modelos de esta enfermedad.
BPAN es un trastorno genético raro ligado al cromosoma X que provoca una acumulación anómala de hierro en el cerebro y afecta gravemente al sistema nervioso. Sus síntomas incluyen convulsiones recurrentes, discapacidad intelectual, retraso en el desarrollo, ataxia y parkinsonismo. Actualmente, no existe un tratamiento curativo, y las opciones disponibles solo alivian parcialmente los síntomas.
Reactivar el cromosoma X para restaurar funciones celulares
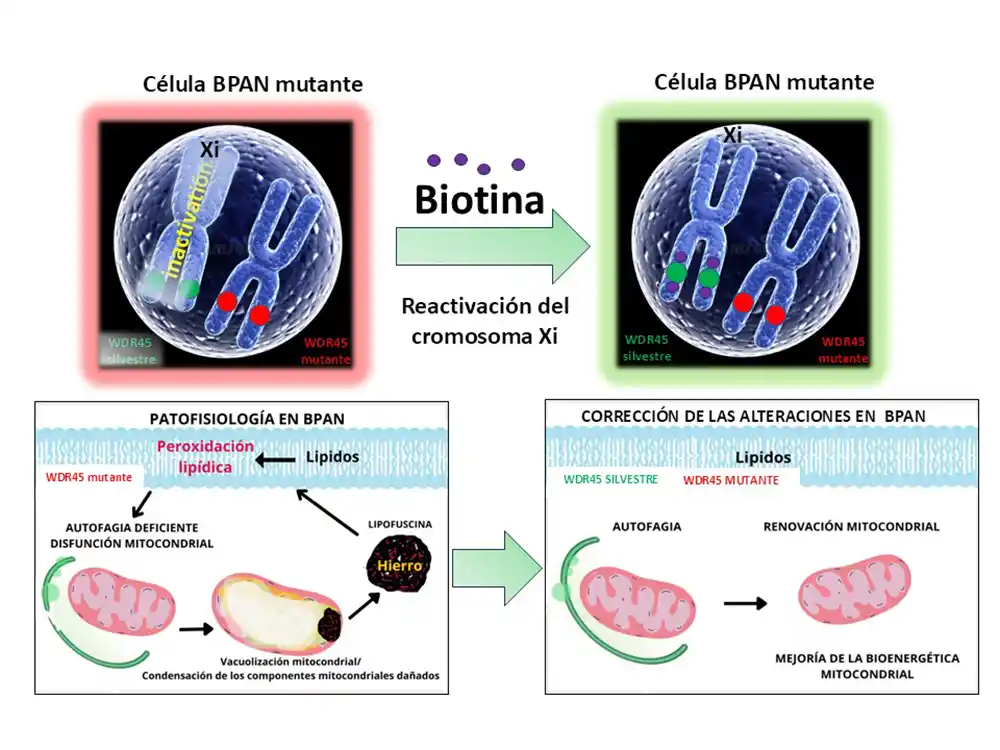
El equipo del CABD ha descubierto que la biotina es capaz de restaurar la expresión del gen WDR45, cuya mutación provoca la enfermedad. Este proceso ocurre gracias a la biotinilación de las histonas, un mecanismo epigenético que favorece la reactivación del cromosoma X inactivo, permitiendo que el alelo funcional del gen vuelva a expresarse. Los resultados muestran una mejora notable en la homeostasis del hierro, la bioenergética mitocondrial y la capacidad autofágica de las células, aspectos clave en el desarrollo de BPAN.
Según el Dr. Sánchez Alcázar, “nuestros resultados indican que la reactivación del cromosoma X inactivo no solo representa una nueva vía terapéutica para BPAN, sino que también podría aplicarse a otras enfermedades genéticas ligadas a este cromosoma, como el síndrome de Rett o el síndrome del cromosoma X frágil”.
La investigación ha sido posible gracias al respaldo de asociaciones de pacientes como ‘Camina con Lola’, ‘Gabriella mi pequeña guerrera’ y ‘BPAN Spain’, así como de la Fundación Bancaria Unicaja.
Un paso más en la medicina personalizada
Este hallazgo se enmarca en el Proyecto BrainCure, una iniciativa que desde 2014 apuesta por la medicina personalizada para enfermedades neurodegenerativas con acumulación de hierro. El equipo evalúa tratamientos en modelos celulares derivados de pacientes, lo que permite seleccionar las opciones más efectivas antes de su posible aplicación clínica. Actualmente, este enfoque se está utilizando con más de 40 pacientes de distintos países, incluyendo España, Brasil, México y Estados Unidos.
El Proyecto BrainCure está realizando medicina de precisión en los 5 subtipos más frecuentes: PKAN, neurodegeneración asociada a pantotenato kinasa, con mutaciones en el gen PANK2; PLAN, neurodegeneración asociada a PLA2G6, con mutaciones en el gen PLA2G6; BPAN, neurodegeneración asociada a la proteína beta-propeller, con mutaciones en el gen WDR45; MPAN, neurodegeneración asociada a la proteína de la membrana mitocondrial, con mutaciones en el gen C19orf12; y FAHN, neurodegeneración asociada a la hidroxilasa de ácidos grasos, con mutaciones en el gen FA2H.















